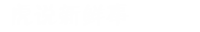科学探索|比mRNA疫苗更优?北大团队开发环状RNA疫苗:对奥密克戎等广谱( 二 )
与线性的mRNA不同,环状RNA分子呈共价闭合环状结构,不含5-Cap和3’-polyA结构;且不需要引入修饰碱基, 其稳定性高于线性RNA 。环状RNA是非编码RNA中的一大类,它由一种非经典剪接方式即反向剪接(backsplicing)产生 。其发现于1976年,并在近几年里成为了新一代的明星分子 。
研究团队指出,相比之下,环状RNA由于其共价封闭的环结构而高度稳定,这可以保护其免受外切酶介导的降解 。据此前报道,环状RNA比线性mRNA更稳定,在哺乳动物细胞中,环状RNA的中位半衰期至少比线性mRNA长2.5倍 。
不过,迄今为止,只有少数内源性环状RNA被证明具有蛋白质翻译模板的功能 。天然的环状RNA因为没有5’端的帽子结构,一般无法进行翻译 。不过,它可以通过内部核糖体进入位点(IRES)或加入开放阅读框(ORF)上游的m6A修饰来实现蛋白质翻译 。
因此,研究团队设想,环状RNA可以作为一个产生免疫原的平台 。魏文胜等人也同时指出,RNA的环化方法、纯化策略尚不成熟,其潜在的免疫原性对疫苗研发的影响并不清楚,诸多未知因素也制约着环状RNA的研发应用 。
魏文胜对澎湃新闻采访人员表示,其团队环状RNA疫苗的研发工作在疫情暴发后启动 。
论文显示,研究团队采用Group I核酶自催化策略来产生编码SARS-CoV-2 RBD抗原的环状RNA,称为circRNA^RBD 。为了增强RBD抗原的免疫原性,在RBD的N端添加了信号肽序列(SP),以实现其分泌表达 。在这个结构中,内部核糖体进入位点(IRES)元素置于RBD编码序列之前以启动其翻译 。为了增强RBD抗原的免疫原性,他们还将人组织型纤溶酶原激活物(tPA)的信号肽序列融合到RBD的N端,以确保抗原的分泌 。
此外,鉴于S蛋白三聚体在结合hACE2方面表现优于单体S蛋白,同时为提高RBD抗原的免疫原性,将T4噬菌体纤维蛋白(Foldon)的三聚化基序融合到其C端 。然后将该IRES-SP-RBD-Foldon序列插入环化载体,构建用于产生circRNA^RBD的体外转录(IVT)模板 。
初步显示:设计疫苗有效中和奥密克戎株在内的多种变异株
魏文胜等人提到,实验证明,编码新冠病毒刺突蛋白RBD的环状RNA疫苗可以在小鼠和恒河猴体内诱导产生高水平的新冠病毒中和抗体以及特异性T细胞免疫反应,并可以有效降低新冠病毒感染的恒河猴肺部的病毒载量,显著缓解新冠病毒感染引起的肺炎症状 。

文章图片
CircRNA疫苗接种在小鼠和恒河猴体内提供了显著性保护 。一系列的对比评估表明,与mRNA疫苗相比,circRNA疫苗具有以下特点或优势:circRNA具有更高的稳定性,可以在体内产生更高水平、更加持久的抗原;circRNA疫苗诱导机体产生的中和抗体比例更高,可以更有效地对抗病毒变异,降低疫苗潜在的抗体依赖增强症(ADE)副作用;circRNA疫苗诱导产生的IgG2/IgG1的比例更高,表明其主要诱导产生Th1型保护性T细胞免疫反应,可以有效降低潜在的疫苗相关性呼吸道疾病(VAERD)副作用 。
文章图片
CircRNA疫苗的特点和优势(相比于mRNA疫苗) 。此外,值得一提的是,在奥密克戎突变株被世界卫生组织(WHO)列为值得关注的变异株(VOC)后,研究团队还紧急启动了针对该突变株的环状RNA疫苗研发 。
在获得病毒序列信息的30天内,研究团队完成了从疫苗生产、小鼠免疫到有效性评估的全流程 。研究发现,基于奥密克戎变异株的环状RNA疫苗(circRNA^RBD-Omicron)的保护范围狭窄,其诱导产生的抗体只能够中和奥密克戎变异株 。
- 科学探索|科学家研发毫米级机器人 可实现人体内靶向给药
- 科学探索|野生蝙蝠被发现可在4年后识别跟食物奖励相关的铃声
- 科学探索|盘点大自然6种能使身体部位再生的动物
- 科学探索|中国空间站的光学舱:巡天空间望远镜预计2024年投入科学运行
- 科学探索|科学家发现了本质上不会衰老的物种
- 科学探索|问天实验舱器箭组合体今天进行垂直转运
- 科学探索|新研究揭示了大象是如何避免癌症的
- 科学探索|一种新开发的抗生素被发现可以杀死耐药性细菌
- 科学探索|增材纺织法造出人工心室模型
- 科学探索|MIT团队找到改善工业沸水工艺的方法